Ce reprezintă definiția produselor farmaceutice ne-medicamentoase în cadrul Legii Japoneze a Dispozitivelor Medicale și Farmaceutice? Despre eficacitatea și beneficiile care pot fi exprimate în publicitate
Verificarea conformității cu Legea Japoneză a Dispozitivelor și Produselor Farmaceutice este o activitate de gestionare a riscurilor care se desfășoară în mod regulat în companiile de producție și magazinele de medicamente care se ocupă cu produse farmaceutice ne-medicale. Cu toate acestea, standardele pentru afișarea publicității permise de Legea Japoneză a Dispozitivelor și Produselor Farmaceutice sunt ambigue, ceea ce face dificilă luarea deciziilor și există cazuri în care se încalcă legea fără intenție.
Acest articol va explica cum să exprimați în mod corespunzător eficacitatea și efectele cerute în etapa de aplicare și publicitate pentru produsele farmaceutice ne-medicale, pentru a preveni încălcările neintenționate ale Legii Japoneze a Dispozitivelor și Produselor Farmaceutice, explicat de un avocat.
Ce înseamnă “produse farmaceutice ne-medicamentoase” în cadrul Legii Dispozitivelor Medicale și Farmaceutice
Articolul 2, alineatul 2 din Legea Dispozitivelor Medicale și Farmaceutice (Legea Japoneză privind calitatea, eficacitatea și siguranța produselor farmaceutice și a dispozitivelor medicale) definește “produsele farmaceutice ne-medicamentoase” în felul următor.
În această lege, “produse farmaceutice ne-medicinale” se referă la obiectele enumerate mai jos care au un efect blând asupra corpului uman.
1. Obiecte care nu sunt aparate mecanice și sunt utilizate în scopurile enumerate de la A la C (excluzând obiectele care sunt utilizate și pentru scopurile prevăzute la punctele 2 sau 3 din paragraful anterior).
A. Prevenirea grețurilor și a altor disconforturi sau a halenei sau a mirosului corporal
B. Prevenirea transpirației, a iritațiilor etc.
C. Prevenirea căderii părului, stimularea creșterii părului sau îndepărtarea părului
2. Obiecte care nu sunt aparate mecanice și sunt utilizate pentru scopul de a preveni organisme precum șoarecii, muștele, țânțarii, puricii și altele asemenea, pentru sănătatea oamenilor sau a animalelor (excluzând obiectele care sunt utilizate și pentru scopurile prevăzute la punctele 2 sau 3 din paragraful anterior).
3. Obiecte care sunt utilizate pentru scopurile prevăzute la punctele 2 sau 3 din paragraful anterior (excluzând obiectele enumerate la punctul 2) și care sunt desemnate de Ministrul Sănătății, Muncii și Bunăstării.
Prin urmare, “produsele farmaceutice ne-medicinale” sunt cele care au un efect asupra corpului uman care se situează între “medicamente” și “cosmetice” și care sunt mai blânde decât medicamentele. De exemplu, cosmeticele medicinale, băuturile nutritive, vopselele de păr, pastele de dinți medicinale, spray-urile antiperspirante, produsele pentru creșterea părului și insecticidele sunt considerate “produse farmaceutice ne-medicinale”.
De asemenea, produsele care au trecut de la “medicamente” la “produse farmaceutice ne-medicinale” ca urmare a modificării “Ordonanței de punere în aplicare a Legii farmaceutice” din anul Heisei 11 (1999) sunt numite “produse farmaceutice ne-medicinale nou desemnate”, iar cele care au trecut ca urmare a modificării din anul Heisei 16 (2004) sunt numite “produse farmaceutice ne-medicinale cu noua gamă”. Acestea sunt incluse în “produsele farmaceutice ne-medicinale desemnate” prevăzute la punctul 3 al alineatului 2 al articolului 2 din Legea privind dispozitivele medicale și farmaceutice.
“Produsele farmaceutice ne-medicinale” conțin ingrediente active eficiente pentru efectele și beneficiile desemnate și aprobate de Ministerul Sănătății, Muncii și Bunăstării, la o anumită concentrație, și sunt create mai degrabă pentru “prevenire” decât pentru “tratament” al bolilor etc. În plus, termenul “medicinal” este permis doar pentru “produsele farmaceutice ne-medicinale”, care au un efect mai blând decât medicamentele, deci “medicinal = produs farmaceutic ne-medicinal”.
Agenția Națională pentru Medicamente și Dispozitive Medicale (PMDA) explică definiția și caracteristicile “produselor farmaceutice ne-medicinale” în felul următor:
1. Efectul asupra corpului uman este moderat. (Articolul 2, alineatul 2 din Legea japoneză a dispozitivelor farmaceutice)
2. Nu este un medicament. (Articolul 2, alineatele 1 și 2 din Legea japoneză a dispozitivelor farmaceutice, Notificarea Directorului nr. 464 din 6 septembrie 1962 (Anul 37 al erei Showa))
① Pentru cele care depășesc limita ca produs farmaceutic non-medicamentos în ceea ce privește ingredientele și cantitatea sau esența, acestea sunt tratate ca medicamente, indiferent de eficacitatea sau efectul lor.
② Chiar și pentru cele care sunt în limita recunoscută ca produs farmaceutic non-medicamentos în ceea ce privește ingredientele și cantitatea sau esența, acestea sunt tratate ca medicamente dacă eficacitatea, efectul sau modul de utilizare și dozajul depășesc limita ca produs farmaceutic non-medicamentos.
3. Produsul nu este unul dintre cele enumerate mai jos. (Notificarea Directorului nr. 464 din 6 septembrie 1962 (Anul 37 al erei Showa))
a. Substanțe care corespund otrăvurilor sau drogurilor puternice
b. Produse pure
4. Scopul principal al utilizării este “prevenirea”. (Notificarea Directorului nr. 464 din 6 septembrie 1962 (Anul 37 al erei Showa) etc.)
※ Pentru produsele farmaceutice non-medicamentoase nou desemnate și cele cu un nou domeniu, consultați notificările relevante etc.
5. Este un produs care se presupune că va fi utilizat în mod continuu în viața de zi cu zi.
6. În principiu, nu se presupune că va fi utilizat sub supravegherea profesioniștilor din domeniul medical, cum ar fi medicii sau farmaciștii.
“Considerații de bază la solicitarea aprobării pentru produsele farmaceutice non-medicamentoase (ediția 2021)”[ja]
Pentru criteriile de clasificare a medicamentelor etc. în Legea japoneză a dispozitivelor farmaceutice, consultați articolul de mai jos pentru o explicație detaliată.
Articol de referință: “Ce este Legea dispozitivelor farmaceutice (fosta Lege a afacerilor farmaceutice)? Explicăm scopul, obiectul reglementării și reglementările privind publicitatea”[ja]
Diferența dintre cosmeticele generale și produsele farmaceutice ne-medicinale
“Cosmeticele” sunt clasificate în “cosmetice generale” și “cosmetice medicinale” (un tip de produs farmaceutic ne-medicinal) conform legii japoneze privind dispozitivele și medicamentele farmaceutice.
Definiția “cosmeticelor” este stabilită în alineatul 3 al articolului 2 din Legea japoneză privind dispozitivele și medicamentele farmaceutice, după cum urmează:
În această lege, termenul “cosmetic” se referă la produsele care sunt utilizate pentru a curăța corpul uman, a-l înfrumuseța, a-i crește atractivitatea, a-i schimba aspectul sau a menține pielea sau părul sănătos, prin aplicare pe corp, pulverizare sau alte metode similare. Acestea includ produsele care au un efect blând asupra corpului uman. Cu toate acestea, nu sunt incluse produsele care, pe lângă aceste scopuri de utilizare, sunt utilizate și pentru scopurile prevăzute la punctele 2 sau 3 ale alineatului (1), precum și produsele farmaceutice non-medicinale.
Prin urmare, “cosmeticele (cosmeticele generale)” sunt produsele care sunt utilizate cu scopul de a curăța corpul, a-l înfrumuseța, a-i crește atractivitatea, a menține pielea sau părul sănătos, etc., comparativ cu “medicamentele” și “produsele farmaceutice non-medicinale”, având un efect blând.
În cazul “cosmeticelor generale”, Ministerul Sănătății, Muncii și Protecției Sociale a stabilit 56 de efecte care pot fi afișate pe ambalajul produsului, cum ar fi “previne iritațiile pielii” sau “curăță cavitatea bucală”. Dacă se face publicitate care depășește aceste limite, se încalcă Legea privind dispozitivele medicale și farmaceutice.
Pe de altă parte, “cosmeticele medicinale” conțin “ingrediente active” care au efecte precum prevenirea problemelor pielii, acnee, albire, deodorant, etc., și pot promova efectele fiecărui ingredient activ. Ministerul Sănătății, Muncii și Protecției Sociale a clasificat cosmeticele medicinale în 8 categorii, în funcție de tipul de produs, după ce a specificat ingredientele active, și a stabilit domeniul de eficacitate care poate fi promovat de fiecare grup de produse. Detalii vor fi explicate în capitolul următor.
De asemenea, în cazul “cosmeticelor medicinale”, este necesar să se afișeze “produs farmaceutic non-medicinal” pe ambalajul produsului. În plus, în timp ce “cosmeticele generale” sunt obligate să afișeze toate ingredientele conform Legii privind dispozitivele medicale și farmaceutice, “produsele farmaceutice non-medicinale” sunt suficiente dacă afișează doar “ingredientele specificate pentru afișare” conform Legii privind dispozitivele medicale și farmaceutice, iar diferența este că afișează toate ingredientele conform standardelor voluntare ale Asociației Industriale a Cosmetice din Japonia.
“Legea privind dispozitivele medicale și farmaceutice” reglementează în principal cinci categorii: medicamente, produse farmaceutice non-medicinale, cosmetice, dispozitive medicale și produse pentru medicina regenerativă. Dintre acestea, am rezumat definițiile medicamentelor și cosmeticelor generale, care sunt ușor de confundat cu produsele farmaceutice non-medicinale, și clasificarea în fiecare categorie în tabelul de mai jos.
【Clasificarea conform Legii privind dispozitivele medicale și farmaceutice】
| Medicamente | Produse farmaceutice non-medicinale | Cosmetice | |
| Definiție | 1. Cele incluse în Farmacopeea Japoneză. 2. Cele utilizate pentru diagnosticarea, tratamentul sau prevenirea bolilor la oameni sau animale. 3. Cele utilizate pentru diagnosticarea, prevenirea sau tratamentul bolilor și care au ca scop afectarea structurii sau funcției corpului. (Legea privind dispozitivele medicale și farmaceutice, articolul 2, alineatul 1) | 1. Cele cu un efect blând asupra corpului uman și care au ca scop prevenirea mirosului corporal, transpirației, căderii părului, etc. 2. Cele utilizate pentru a preveni organisme dăunătoare pentru sănătatea umană sau animală. 3. Cele specificate de Ministrul Sănătății, Muncii și Protecției Sociale și utilizate în același scop ca medicamentele. (Legea privind dispozitivele medicale și farmaceutice, articolul 2, alineatul 2) | Cele cu un efect blând asupra corpului uman și care au ca scop îngrijirea sau protecția gurii, pielii, părului, unghiilor, colorarea sau parfumarea. (Legea privind dispozitivele medicale și farmaceutice, articolul 2, alineatul 3) |
| Clasificare în cadrul categoriei | 1. Medicamente pentru uz medical (Medicamente pe bază de rețetă) 2. Medicamente care necesită îndrumare 3. Medicamente pentru uz general (Medicamente OTC) | 1. Produse farmaceutice non-medicinale generale (Cosmetice medicinale, etc.) 2. Produse farmaceutice non-medicinale specificate | Cosmetice generale |
| Aprobarea fabricării și vânzării | Este necesară aprobarea Ministrului Sănătății, Muncii și Protecției Sociale, etc. | Este necesară aprobarea Ministrului Sănătății, Muncii și Protecției Sociale, etc. | Aprobarea nu este necesară în principiu |
Despre eficacitatea și efectele care pot fi exprimate prin produsele farmaceutice non-medicinale

În cazul “produselor farmaceutice non-medicinale” (Japanese “医薬部外品”), Ministerul Sănătății, Muncii și Protecției Sociale din Japonia a stabilit gama de eficacitate și efecte care pot fi afișate în funcție de tipul produsului farmaceutic non-medicinal. Dacă se face publicitate care depășește această gamă, se va încălca Legea privind dispozitivele și produsele farmaceutice (Japanese “薬機法”).
Exprimarea efectelor diferite între cosmeticele generale și cele medicinale
După cum am menționat mai devreme, cosmeticele medicinale, care sunt produse farmaceutice non-medicinale, pot promova nu numai efectele benefice ale ingredientelor active desemnate, dar și cele 56 de efecte benefice care pot fi afișate în cosmeticele generale. Prin urmare, acestea pot realiza publicitate mai persuasivă decât cosmeticele generale.
【Diferențele între cosmeticele generale și produsele farmaceutice non-medicinale】
| Cosmetice generale | Cosmetice medicinale | |
| Gama de efecte benefice | 56 de efecte benefice desemnate de Ministerul Sănătății, Muncii și Bunăstării | Efecte benefice aprobate + efecte benefice ale cosmeticele generale |
| Includerea ingredientelor active | Nu | Da |
Există trei aspecte de care trebuie să țineți cont atunci când cosmeticele medicinale promovează aceleași efecte benefice (cele 56 de efecte benefice desemnate de Ministerul Sănătății, Muncii și Bunăstării) ca și cosmeticele generale:
- Să nu se creeze impresia greșită că este un produs cosmetic, ascunzând scopul original al produsului farmaceutic non-medicinal.
- Să nu fie un produs care ar putea cauza probleme de sănătate și igienă dacă este utilizat în scopuri și metode cosmetice (de exemplu, șampon cu agent antibacterian sau săpun medicinal).
- Să nu se creeze impresia greșită că efectul benefic respectiv a fost aprobat ca efect benefic al produsului farmaceutic non-medicinal.
Pentru criteriile detaliate de judecată asupra dacă efectele benefice și exprimarea în publicitatea produselor farmaceutice non-medicinale, inclusiv cosmeticele medicinale, încalcă Legea privind dispozitivele și produsele farmaceutice (Japanese Pharmaceutical Affairs Law), vă rugăm să consultați “Explicații și puncte de atenție privind standardele adecvate de publicitate pentru produsele farmaceutice, etc.”[ja] ale Ministerului Sănătății, Muncii și Bunăstării sau “Ghidul pentru publicitatea adecvată a produselor cosmetice, etc.”[ja] al Asociației Industriale a Cosmetice din Japonia.
Exemple de expresii care încalcă Legea Japoneză a Dispozitivelor Farmaceutice și Medicale
Un cuvânt cheie bine cunoscut care poate încălca reglementările privind Legea Japoneză a Dispozitivelor Farmaceutice și Medicale și publicitatea medicală este “anti-îmbătrânire”.
Anti-îmbătrânire (în engleză: Anti-Aging) este un termen care înseamnă “prevenirea și vindecarea simptomelor asociate cu îmbătrânirea, prevenirea îmbătrânirii, anti-îmbătrânire, anti-îmbătrânire”.
Ministerul Sănătății, Muncii și Bunăstării din Japonia a exprimat următoarea opinie cu privire la termenul “anti-îmbătrânire” în “Ghidul pentru publicitatea medicală”[ja] (publicat pe 8 mai în anul Heisei 30 (2018)).
Clinicile anti-îmbătrânire sau (simplu) anti-îmbătrânire nu sunt recunoscute ca nume de specialitate medicală, iar tratamentele lor nu sunt acoperite de asigurările medicale publice sau aprobate conform Legii Japoneze a Dispozitivelor Medicale și Farmaceutice. De asemenea, acestea nu pot fi promovate prin publicitate.
De asemenea, în decembrie 2018 (anul 30 al erei Heisei, 2018 în calendarul gregorian), în „Rezumatul discuțiilor Grupului de lucru pentru îngrijire medicală și asistență socială, ediția a 4-a”[ja] se menționează următoarele (am modificat unele expresii din textul original pentru a se potrivi cu contextul):
„Ministerul Sănătății, Muncii și Bunăstării nu interzice în mod absolut utilizarea termenului ‘anti-îmbătrânire’, dar nu poate aproba utilizarea acestuia pentru a atrage pacienți. Cu toate acestea, dacă se îndeplinesc anumite condiții, se poate furniza informații despre acesta, chiar dacă nu este inclus în ‘elementele care pot fi publicitate’.„
Având în vedere cele de mai sus, utilizarea termenului ‘anti-îmbătrânire’ în publicitatea medicală este în principiu interzisă. Cu toate acestea, în cazul în care se îndeplinesc cerințele specifice de relaxare a restricțiilor din Ghidul de publicitate medicală, acesta poate fi excepțional acceptat ca descriere a procedurilor medicale. De asemenea, ‘anti-îmbătrânire’ nu poate fi utilizat în publicitatea pentru produsele farmaceutice deoarece implică un efect terapeutic sau farmaceutic.
Pe de altă parte, există termeni similari, cum ar fi ‘îngrijirea îmbătrânirii’ sau ‘măsuri împotriva îmbătrânirii’, care, spre deosebire de ‘anti-îmbătrânire’, nu implică proceduri medicale sau efecte terapeutice sau farmaceutice. Prin urmare, acestea pot fi utilizate în publicitatea pentru produsele farmaceutice, dacă se încadrează în limitele efectelor aprobate.
‘Îngrijirea îmbătrânirii’ se referă la îngrijirea cu produse cosmetice adecvate vârstei. În publicitatea pentru produsele farmaceutice, nu se poate utiliza termenul ‘îngrijirea îmbătrânirii’ cu scopul de a promova ‘tratamentul’ sau ‘îmbunătățirea’ bolilor care sunt clasificate ca efecte terapeutice sau farmaceutice. Acesta poate fi utilizat numai dacă, luând în considerare contextul, se înțelege că se referă la ‘îngrijirea stării pielii în funcție de vârstă’, care este recunoscută ca efect al produselor cosmetice.
Astfel, spre deosebire de ‘anti-îmbătrânire’, care implică proceduri medicale și efecte terapeutice sau farmaceutice, ‘îngrijirea îmbătrânirii’ se referă strict la ‘îngrijirea adaptată stării actuale’, ceea ce o face mai compatibilă cu produsele cosmetice și produsele farmaceutice.
De asemenea, termenii ‘albire’ și ‘înălbire’ pot fi utilizați dacă sunt respectate anumite reguli, cum ar fi utilizarea lor împreună cu efecte de machiaj sau alte restricții.
Pentru exemple concrete de utilizare a fiecărui termen permis de reglementările Legii Japoneze a Dispozitivelor Medicale și Farmaceutice, vă rugăm să consultați „Ghidul pentru publicitatea corectă a produselor cosmetice etc.”[ja].
Articol de referință: Puncte de atenție în exprimarea publicității pentru produsele cosmetice și alimentele sănătoase[ja]
Puncte de atenție la fabricarea și vânzarea produselor farmaceutice non-medicinale

În cazul fabricării și vânzării produselor farmaceutice non-medicinale, este necesară aprobarea sau autorizarea Ministrului Sănătății, Muncii și Bunăstării sau a guvernatorilor fiecărei prefecturi. Aici, vom explica punctele de bază de care trebuie să țineți cont atunci când obțineți permisiunile necesare în procesul de distribuție a produselor farmaceutice non-medicinale.
În primul rând, pentru a fabrica și a vinde (expedia) produse farmaceutice non-medicinale, este necesar să obțineți permisiunea de fabricație și permisiunea de fabricație și vânzare de la guvernatorul fiecărei prefecturi (Articolul 12 și Articolul 13 din Legea japoneză a dispozitivelor farmaceutice și medicale, Paragraful 2 al Articolului 80 din Ordonanța de punere în aplicare a Legii dispozitivelor farmaceutice și medicale). De asemenea, pentru a fabrica produse farmaceutice non-medicinale în străinătate, este necesar să obțineți recunoașterea producătorului străin de la Ministrul Sănătății, Muncii și Bunăstării (Articolul 13 al 3-lea din Legea japoneză a dispozitivelor farmaceutice și medicale).
De asemenea, atunci când fabricați și vindeți efectiv produse farmaceutice non-medicinale, trebuie să depuneți o cerere de aprobare de fabricație și vânzare pentru fiecare produs la autoritatea de reglementare (Ministrul Sănătății, Muncii și Bunăstării sau guvernatorul fiecărei prefecturi) și să obțineți aprobarea pentru siguranță, eficacitate și calitate (Articolul 14 din Legea japoneză a dispozitivelor farmaceutice și medicale).
Aplicațiile pentru diverse permisiuni prezentate mai sus sunt făcute la guvernatorul prefecturii în care se află locul de fabricație sau biroul de vânzări. Pe de altă parte, cererile de aprobare pentru fiecare produs sunt făcute fie la Ministrul Sănătății, Muncii și Bunăstării, fie la guvernatorul prefecturii (pentru produsele farmaceutice non-medicinale care nu sunt cosmetice medicinale, o parte din autoritatea de aprobare este delegată guvernatorilor prefecturilor).
Clasificarea aplicațiilor pentru “produse farmaceutice non-medicinale” este împărțită în 11 categorii în funcție de ingredientele, cantitatea, eficacitatea, efectele etc. care sunt combinate, iar tipul de documente atașate necesare variază, așa că este necesară atenție.
Pentru detalii, vă rugăm să consultați “Procedura de fabricație și vânzare a produselor farmaceutice non-medicinale” publicată de Organizația Independentă Administrativă pentru Dispozitive Medicale și Farmaceutice (PMDA) aici.
Pentru fluxul fiecărei aplicații de permisiune și aprobare, vă rugăm să consultați diagrama de mai jos.
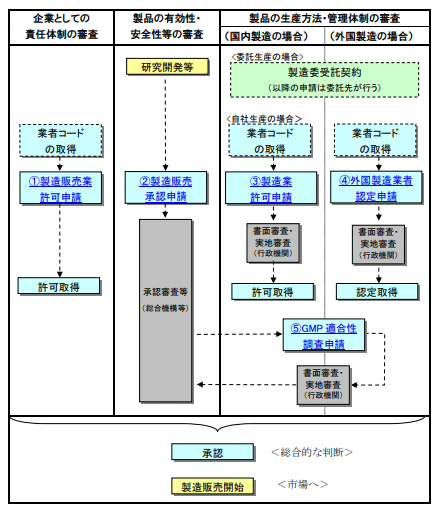
“Procedura de fabricație și vânzare a produselor farmaceutice non-medicinale”[ja]
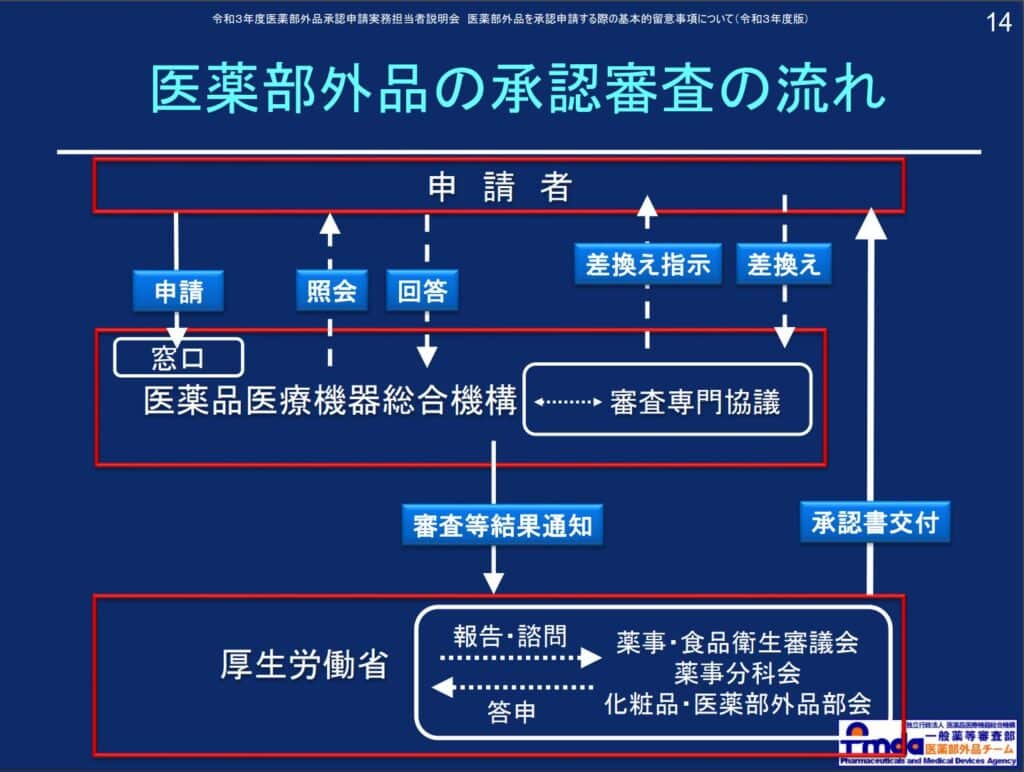
De asemenea, pentru ingredientele active care pot fi incluse în “cosmetice medicinale” și “produse farmaceutice non-medicinale”, vă rugăm să consultați “Lista ingredientelor active în așa-numitele cosmetice medicinale” publicată de Ministerul Sănătății, Muncii și Bunăstării aici[ja].
În plus, există 140 de substanțe chimice selectate pentru ingredientele specificate pentru afișare (ingredientele anunțate) care sunt obligatorii pentru “produse farmaceutice non-medicinale”. Pentru detalii, vă rugăm să consultați “Ingredientele produselor farmaceutice non-medicinale și cosmeticele desemnate de Ministrul Sănătății, Muncii și Bunăstării” aici[ja].
Concluzie: Verificarea legală a Legii Farmaceutice trebuie făcută de un avocat
În urma modificărilor aduse Legii Farmaceutice în primul an al erei Reiwa (2019), s-a instituit un sistem de amenzi administrative ca măsură de reglementare a publicității pentru medicamente, ceea ce a înăsprit pedepsele pentru încălcarea reglementărilor de publicitate ale Legii Farmaceutice. Ghidurile de publicitate pentru medicamente sunt revizuite anual, iar cei implicați în operarea și examinarea publicității pentru medicamente, cum ar fi companiile și agențiile de publicitate, sunt solicitați să acționeze cu prudență.
Interpretarea Legii Farmaceutice și determinarea dacă exprimarea în publicitate este adecvată pot fi dificile de auto-evaluat, așa că dacă aveți nelămuriri, vă recomandăm să consultați un avocat care este familiarizat cu verificarea legală a Legii Farmaceutice.
Verificarea legală a Legii Farmaceutice și propunerea de reexprimare sunt domenii cu un grad ridicat de specializare. Biroul nostru de avocatură Monolis a format o echipă juridică specializată în Legea Farmaceutică, care se ocupă cu verificarea articolelor pentru o varietate de produse, de la suplimente alimentare la medicamente.
Orientări privind măsurile luate de biroul nostru
Biroul nostru de avocatură Monolith este o firmă de avocatură cu o experiență bogată în IT, în special în domeniul internetului și al legii. Oferim servicii precum verificarea legalității articolelor și a paginilor de destinație, crearea de linii directoare și verificarea eșantioanelor pentru operatorii de media, operatorii de site-uri de recenzii, agențiile de publicitate, producătorii de suplimente și cosmetice D2C, clinicile și operatorii de afaceri ASP. Detalii sunt prezentate în articolul de mai jos.
Domeniile de activitate ale Biroului de Avocatură Monolith: Verificarea articolelor și a paginilor de destinație conform legii farmaceutice și a altor legi[ja]
Category: General Corporate





















